Co je mRNA vakcína
Vakcína mRNA přenáší RNA do buněk těla, aby exprimovala a produkovala proteinové antigeny po příslušných modifikacích in vitro, což vede tělo k produkci imunitní odpovědi proti antigenu, čímž se rozšiřuje imunitní kapacita těla.[1,3].
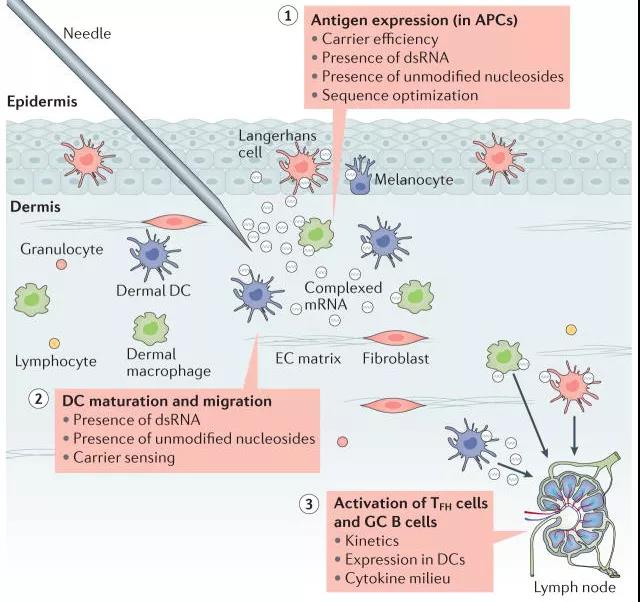
Obrázek 1: Schematický diagram účinku přímé injekce mRNA vakcíny [2]
Klasifikace mRNA vakcín
mRNA vakcíny se dělí na dva typy:nereplikující semRNA asamozesilujícímRNA: samoamplifikující mRNA nejen kóduje cílový antigen, ale také kóduje replikaci, která umožňuje intracelulární amplifikaci RNA a mechanismus exprese proteinu.Nereplikující se mRNA vakcíny pouze kódují cílové antigeny a obsahují 5' a 3' nepřeložené oblasti (UTR).Poskytují komplexní stimulaci adaptability a přirozené imunity, zejména in situ expresi antigenu a přenos nebezpečného signálu, a mají následující aplikace Vlastnosti[2,3]
●Může poskytnout komplexní stimulaci adaptability a vrozené imunity, zejména in situ exprese antigenu a přenosu nebezpečného signálu
●Může vyvolat "vyváženou" imunitní odpověď, včetně humorálních a buněčných efektorů a imunitní paměti
●Může kombinovat různé antigeny bez zvýšení složitosti formulace vakcíny
●Nepřetržitého zlepšování imunitního potenciálu lze dosáhnout opakovanou vakcinací a imunitní odpověď na přenašeče není žádná nebo jen malá
●Tepelně stabilní mRNA vakcíny mohou zjednodušit přepravu a skladování vakcín
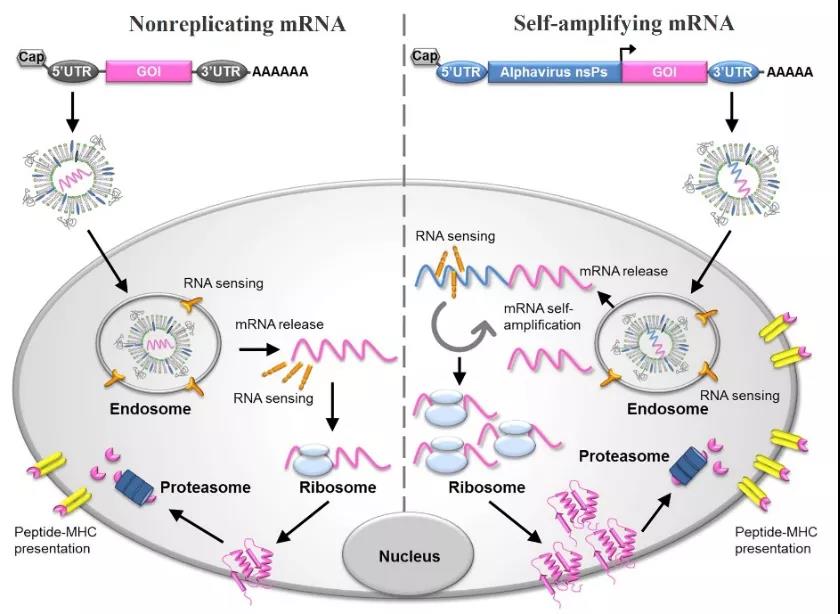
Obrázek 2: Schematický diagram mRNA vakcíny a jejího mechanismu exprese antigenu [4]
Vlastnosti mRNA vakcín
Ve srovnání s tradičními vakcínami mají mRNA vakcíny jednoduché výrobní procesy, vysokou rychlost vývoje, nepotřebují buněčnou kulturu a jsou levné.Ve srovnání s DNA vakcínami nemusejí mRNA vakcíny vstupovat do jádra a není zde riziko integrace do hostitelského genomu.Poločas lze upravit úpravou.
Tabulka 1: Výhody a nevýhody mRNA vakcín
|
| Výhoda | Nedostatek |
| mRNA vakcína | Rychlý výzkum a vývoj, výroba vakcíny trvá pouze 40 dní | Vyvolat zbytečnou imunitní reakci
|
| nestabilita mRNA za fyziologických podmínek, snadno degradovatelná | Neintegruje se do genomu, aby se zabránilo možným terapeutickým mutacím
| |
| Není potřeba žádný jaderný lokalizační signál, transkripce | Zbývá ověřit účinnost bezpečnostního jaderného zařízení
|
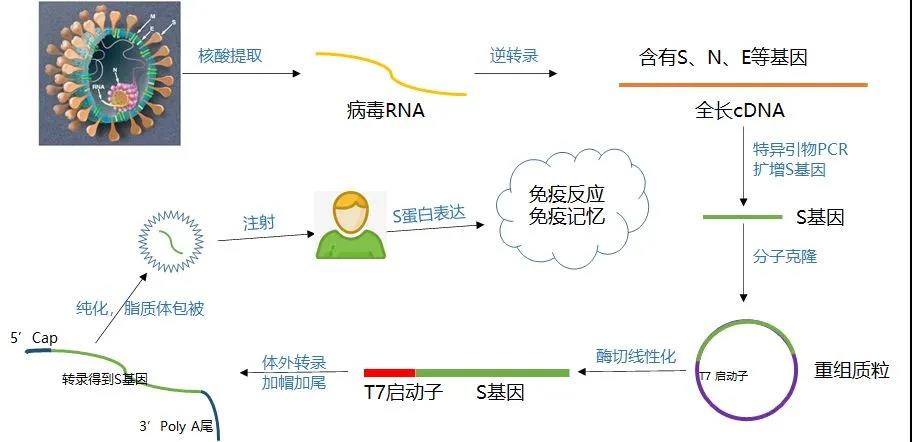
Obrázek 3: Vývojový diagram výroby a přípravy mRNA vakcíny [4]
Foregene Viral RNA Isolation kit
RT-qPCR Easy (jeden krok)
Vylepšené strategie pro přípravu mRNA vakcín
Vzhledem ke špatné stabilitě samotné mRNA, snadné degradaci nukleázami v tkáních, nízké účinnosti vstupu do buněk a nízké účinnosti translace tyto defekty omezují aplikaci mRNA vakcín.Velmi důležitou roli hraje také účinnost překladu.Dodávací vehikula lze rozdělit na virové vektory a nevirové vektory (včetně lipozomů, nelipozomů, virů, nanočástic atd.).Proto jsou potřebná příslušná zlepšení.Následuje strategie farmakologického zlepšení přípravy mRNA[2]
1 Syntetizujte cap analogy nebo použijte capping enzymy ke stabilizaci mRNA a zvýšení translace proteinu vazbou na eukaryotický translační iniciační faktor 4E (EIF4E)
2 Upravte prvky v 5′-nepřeložené oblasti (UTR) a 3′-UTR, abyste stabilizovali mRNA a zvýšili translaci proteinů
3 Přidání Poly(A) ocasu může stabilizovat mRNA a zvýšit translaci proteinu
4 Modifikované nukleosidy pro snížení přirozené imunitní aktivace a zvýšení translace
5 Léčba RNázou III a purifikace rychlou proteinovou kapalinovou chromatografií (FPLC) může snížit imunitní aktivaci a zvýšit translaci
6 Optimalizujte sekvence nebo kodony pro zvýšení translace
7 Společné dodání faktorů iniciace translace a dalších metod ke změně translace a imunogenicity
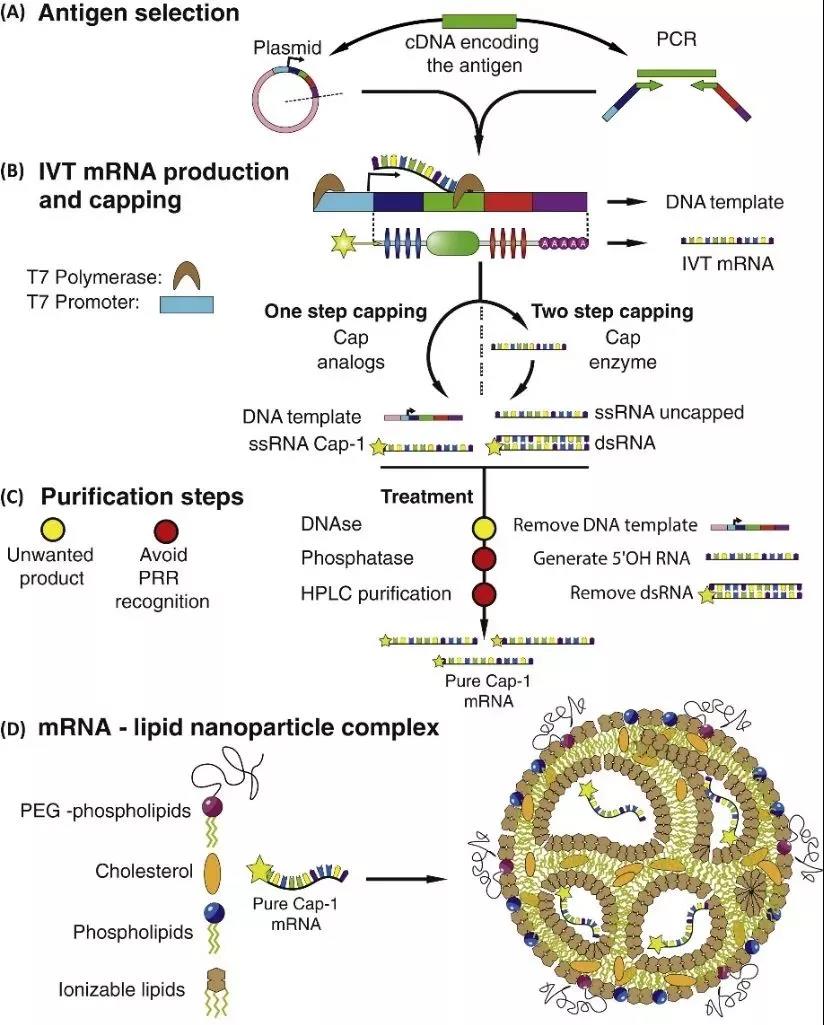
Obrázek 4: Proces produkce a sestavení mRNA in vitro transkripce (IVT) [5]
Příprava plazmidové DNA ve velkém měřítku
Purifikace plazmidové DNA odstraňuje především kontaminanty, jako je RNA, endotoxin DNA s otevřeným kruhem, hostitelský protein a hostitelskou nukleovou kyselinu a obvykle transformuje rekombinantní plazmid na E. coli.E. coli prochází fermentací s vysokou hustotou, poté separací pevná látka-kapalina a sběrem E. coli.E. coli se poté podrobí alkalické lýze, odstředivé separaci pevná látka-kapalina a mikrofiltračnímu čiření po lýze, ultrafiltraci a koncentraci po vyčeření a poté chromatografickému čištění.

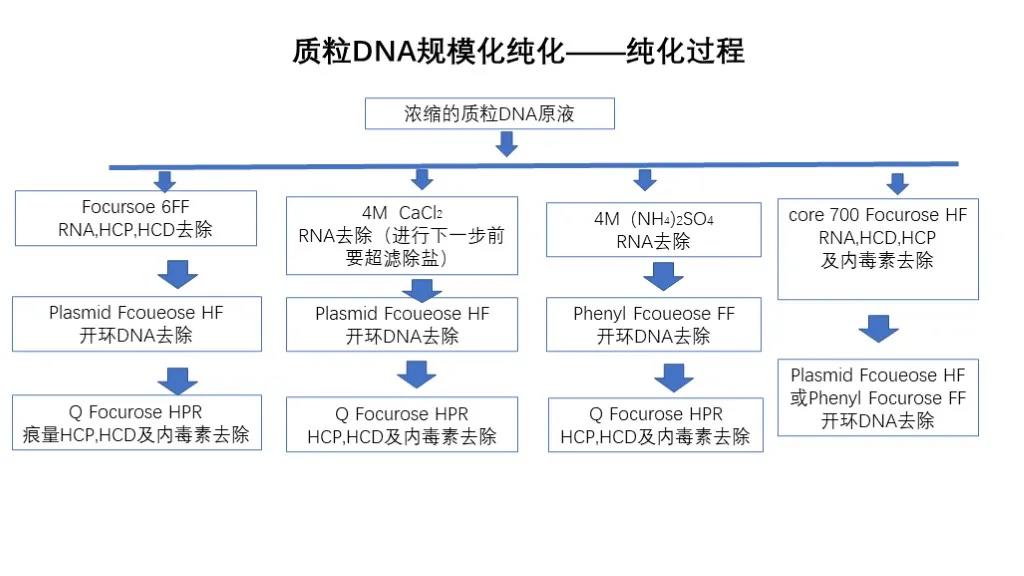
Purifikace plazmidové DNA:
Foregene General Plasmid Mini Kit
【1】苗鹤凡, 郭勇, 江新香.mRNA疫苗研究进展及挑战[J].免疫学杂志, 2016(05):446-449.
【2】Pardi N, Hogan MJ, Porter FW a kol.mRNA vakcíny — nová éra ve vakcinologii[J].Nature Reviews Drug Discovery, 2018.
【3】Kramps T., Elbers K. (2017) Úvod do RNA vakcín.In: Kramps T., Elbers K. (eds.) RNA Vaccines.Methods in Molecular Biology, sv. 1499. Humana Press, New York, NY.
【4】Maruggi G, Zhang C, Li J a kol.mRNA jako transformační technologie pro vývoj vakcín pro kontrolu infekčních onemocnění[J].Molekulární terapie, 2019.
【5】Sergio Linares-Fernández, Céline Lacroix, ,Přizpůsobení mRNA vakcíny k vyvážení přirozené/adaptivní imunitní odpovědi, Trendy v molekulární medicíně, svazek 26, vydání 3, 2020, strany 311-323.
Čas odeslání: srpen-05-2021








