1. Základní znalosti (pokud chcete vidět experimentální část, přeneste si prosím přímo do druhé části)
Jako odvozená reakce konvenční PCR sleduje Real time PCR hlavně změnu množství amplifikačního produktu v každém cyklu amplifikační reakce PCR v reálném čase prostřednictvím změny fluorescenčního signálu a kvantitativně analyzuje výchozí templát prostřednictvím vztahu mezi hodnotou ct a standardní křivkou.
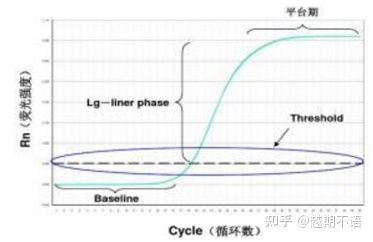
Specifická data RT-PCR jsouzákladní linie, práh fluorescenceaHodnota Ct.
| základní linie: | Hodnota fluorescence 3.-15.cyklu je základní (baseline), která je způsobena občasnou chybou měření. |
| Práh (prah): | Odkazuje na limit detekce fluorescence nastavený ve vhodné poloze v oblasti exponenciálního růstu amplifikační křivky, obecně 10násobek standardní odchylky od základní linie. |
| Hodnota CT: | Je to počet cyklů PCR, kdy hodnota fluorescence v každé reakční zkumavce dosáhne prahové hodnoty. Hodnota Ct je nepřímo úměrná množství počáteční šablony. |
Běžné metody značení pro RT-PCR:
| metoda | výhoda | nedostatek | rozsah použití |
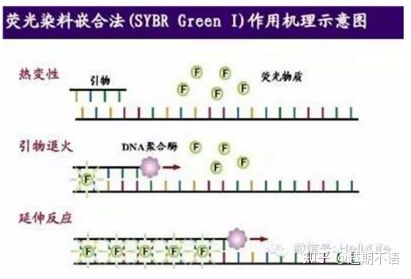
| SYBR ZelenáⅠ | Široká použitelnost, citlivý, levný a pohodlný | Požadavky na primer jsou vysoké, náchylné k nespecifickým pásům | Je vhodný pro kvantitativní analýzu různých cílových genů, výzkum genové exprese a výzkum transgenních rekombinantních zvířat a rostlin. |
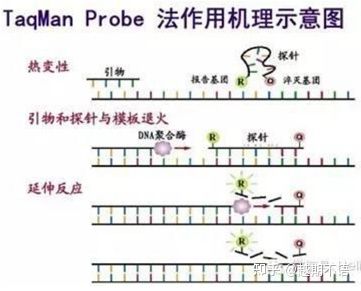
| TaqMan | Dobrá specifičnost a vysoká opakovatelnost | Cena je vysoká a vhodná pouze pro konkrétní cíle. | Detekce patogenů, výzkum genů rezistence na léky, hodnocení účinnosti léků, diagnostika genetických onemocnění. |
| molekulární maják | Vysoká specificita, fluorescence, nízké pozadí | Cena je vysoká, hodí se pouze pro konkrétní účel, provedení je obtížné a cena vysoká. | Analýza specifických genů, analýza SNP |
2. Experimentální kroky
2.1 O experimentálním seskupení- ve skupině musí být více jamek a musí existovat biologická opakování.
| ① | Prázdné ovládání | Používá se k detekci stavu růstu buněk v experimentech |
| ② | Negativní kontrolní siRNA (nespecifická siRNA sekvence) | Ukažte specifičnost působení RNAi.siRNA může vyvolat nespecifickou stresovou reakci v koncentraci 200 nM. |
| ③ | Kontrola transfekčního činidla | Vylučte toxicitu transfekčního činidla pro buňky nebo účinek na expresi cílového genu |
| ④ | siRNA proti cílovému genu | Snižte expresi cílového genu |
| ⑤ (volitelné) | pozitivní siRNA | Používá se k řešení problémů experimentálního systému a provozních problémů |
| ⑥ (volitelné) | Fluorescenční kontrolní siRNA | Účinnost buněčné transfekce lze pozorovat mikroskopem |
2.2 Zásady návrhu primeru
| Velikost zesíleného fragmentu | Výhodně na 100-150 bp |
| Délka primeru | 18-25 bp |
| Obsah GC | 30%-70%, nejlépe 45%-55% |
| Hodnota Tm | 58-60 ℃ |
| Sekvence | Vyhněte se T/C kontinuální;A/G kontinuální |
| 3 koncová sekvence | Vyhněte se GC bohatému nebo AT bohatému;koncová báze je výhodně G nebo C;nejlepší je vyhnout se T |
| Komplementarita | Vyhněte se komplementárním sekvencím o více než 3 bázích v primeru nebo mezi dvěma primery |
| Specifičnost | Pro potvrzení specifičnosti primeru použijte vyhledávání výbuchem |
①SiRNA je druhově specifická a sekvence různých druhů se budou lišit.
②SiRNA je balena v lyofilizovaném prášku, který lze skladovat stabilně po dobu 2-4 týdnů při pokojové teplotě.
2.3 Nástroje nebo činidla, která je třeba připravit předem
| Primer (interní reference) | Včetně dvou vpřed a vzad |
| Primery (cílový gen) | Včetně dvou vpřed a vzad |
| Cílová Si RNA (3 proužky) | Obecně společnost syntetizuje 3 proužky a poté vybere jeden ze tří pomocí RT-PCR |
| Souprava pro transfekci | Lipo2000 atd. |
| Souprava pro rychlou extrakci RNA | Pro extrakci RNA po transfekci |
| Sada pro rychlý zpětný přepis | pro syntézu cDNA |
| PCR Amplification Kit | 2×Super SYBR Green qPCR Master Mix |
2.4 Pokud jde o problémy, kterým je třeba věnovat pozornost v konkrétních experimentálních krocích:
① proces transfekce siRNA
1. Pro nanesení si můžete vybrat 24-jamkovou destičku, 12-jamkovou destičku nebo 6-jamkovou destičku (průměrná koncentrace RNA navrhovaná v každé jamce 24-jamkové destičky je asi 100-300 ng/ul) a optimální hustota transfekce buněk je až 60 %-80 % nebo tak
2. Kroky transfekce a specifické požadavky jsou přísně v souladu s pokyny.
3. Po transfekci lze vzorky odebrat do 24–72 hodin pro detekci mRNA (RT-PCR) nebo detekci proteinů do 48–96 hodin (WB)
② Proces extrakce RNA
1. Zabraňte kontaminaci exogenními enzymy.Zahrnuje především striktní nošení roušek a rukavic;použití sterilizovaných špiček pipet a EP zkumavek;voda použitá v experimentu musí být bez RNázy.
2. Doporučuje se provést dvakrát, než je doporučeno v sadě pro rychlou extrakci, což skutečně zlepší čistotu a výtěžnost.
3. Odpadní kapalina se nesmí dotýkat kolony RNA.
③ Kvantifikace RNA
Poté, co je RNA extrahována, může být kvantifikována přímo pomocí Nanodrop a minimální hodnota může být až 10 ng/ul.
④ Proces reverzní transkripce
1. Vzhledem k vysoké citlivosti RT-qPCR by měly být pro každý vzorek vytvořeny alespoň 3 paralelní jamky, aby se zabránilo tomu, že následná Ct bude příliš odlišná nebo SD nebude příliš velká pro statistickou analýzu.
2. Nezmrazujte a nerozmrazujte Master mix opakovaně.
3. Každá trubice/otvor musí být nahrazena novou špičkou!K přidávání vzorků nepoužívejte neustále stejnou špičku pipety!
4. Film připojený k 96jamkové destičce po přidání vzorku musí být vyhlazený destičkou.Před umístěním na stroj je nejlepší odstředit, aby kapalina na stěně zkumavky mohla stékat dolů a odstranit vzduchové bubliny.
⑤ Společná analýza křivek
| Žádné období logaritmického růstu | Možná vysoká koncentrace šablony |
| Žádná hodnota CT | Nesprávné kroky pro detekci fluorescenčních signálů; degradace primerů nebo sond – její integritu lze detekovat elektroforézou PAGE; nedostatečné množství šablony; degradace šablon – zamezení vnášení nečistot a opakovaného zmrazování a rozmrazování při přípravě vzorků; |
| Ct>38 | Nízká účinnost zesílení;Produkt PCR je příliš dlouhý;různé reakční složky jsou degradovány |
| Lineární křivka zesílení | Sondy mohou být částečně degradovány opakovanými cykly zmrazování a rozmrazování nebo dlouhodobým vystavením světlu |
| Rozdíl v duplicitních otvorech je obzvláště velký | Reakční roztok není zcela roztaven nebo reakční roztok není smíchán;termální lázeň přístroje PCR je kontaminována fluorescenčními látkami |
2.5 O analýze dat
Analýza dat qPCR může být rozdělena na relativní kvantifikaci a absolutní kvantifikaci.Například buňky v léčené skupině ve srovnání s buňkami v kontrolní skupině,
Kolikrát se změní mRNA genu X, to je relativní kvantifikace;v určitém počtu buněk mRNA genu X
Kolik kopií existuje, to je absolutní kvantifikace.Obvykle to, co v laboratoři používáme nejvíce, je relativní kvantitativní metoda.Obvykle,metoda 2-ΔΔctse nejvíce používá v experimentech, proto zde bude podrobně představena pouze tato metoda.
Metoda 2-ΔΔct: Získaný výsledek je rozdíl v expresi cílového genu v experimentální skupině vzhledem k cílovému genu v kontrolní skupině.Je požadováno, aby se účinnost amplifikace jak cílového genu, tak interního referenčního genu blížila 100 % a relativní odchylka by neměla přesáhnout 5 %.
Metoda výpočtu je následující:
Δct kontrolní skupina = hodnota ct cílového genu v kontrolní skupině – hodnota ct vnitřního referenčního genu v kontrolní skupině
Δct experimentální skupina = hodnota ct cílového genu v experimentální skupině – hodnota ct vnitřního referenčního genu v experimentální skupině
ΔΔct=Δct experimentální skupina-Δct kontrolní skupina
Nakonec vypočítejte násobek rozdílu v úrovni výrazu:
Change Fold=2-ΔΔct (odpovídající funkci Excel je POWER)
Související produkty:
Čas odeslání: 20. května 2023